光酶催化不对称羰基羟基化反应

背景
叔醇单元是许多药物和农用化学品中重要的部分。目前获得叔醇单元的方法主要是酮的亲核加成与烯烃的羰基羟基化反应,这两种反应在立体选择性上均存在一定的缺陷。因此,发展出一种不对称催化手段获得叔醇是一个值得探索的课题。
康奈尔大学的Todd K. Hyster团队在此前的研究中,发现黄素依赖的烯还原酶(“ene”-reductases,EREDs)可以通过自由基机理催化C-C键的形成。随后的多项研究中,EREDs完成了各种不对称还原加氢烷基化和加氢磺酰化反应,是一种很有潜力的酶。作者认为,EREDs既然可以催化烯烃的加氢烷基化,那么只要将自由基淬灭的步骤,从还原型变为氧化型,就可以催化烯烃的不对称羰基羟基化,从而制备叔醇类化合物。近日,该团队在JACS上发表《Asymmetric Carbohydroxylation of Alkenes Using Photoenzymatic Catalysis》的一文,就讲述了这样的故事。
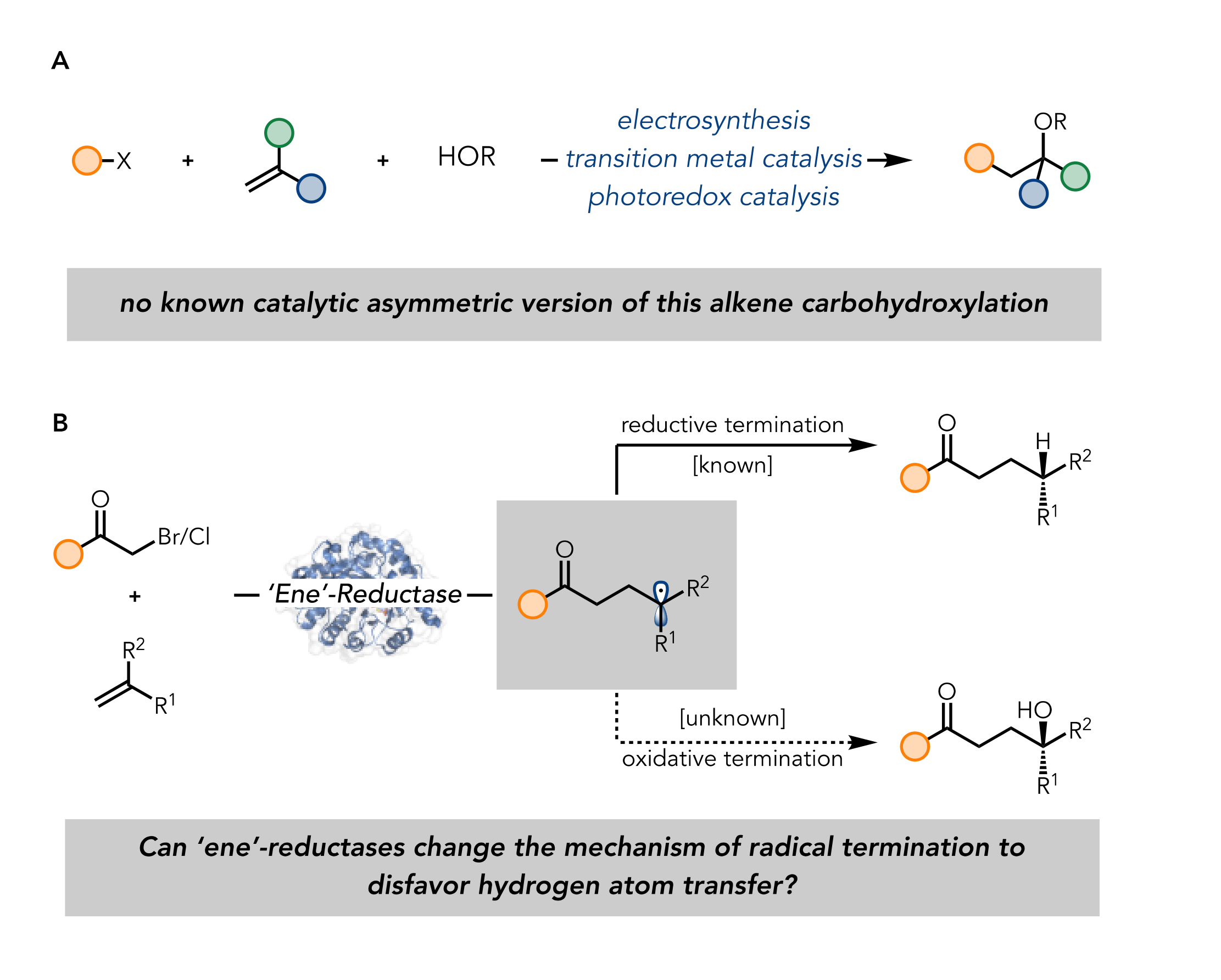
过程
首先,作者对一系列EREDs进行了筛选,发现来源于Pseudomonas putida的吗啡酮还原酶MorB在绿光照射下,可以催化烯烃的羰基羟基化,转化率为45%,对映体比为75:25,副反应产物只占10%。作者遂以MorB为起点,旨在提高转化率和立体专一性。作者选取了催化位点附近的21个氨基酸进行了饱和突变。第一轮饱和突变的最佳效果为转化率提高至83%,对映体比为87:13。第二轮突变中,作者对第一轮中有良好表现的位点进行了细致研究,Y72C突变更换为T使得两个指标分别提高至94%和92:8。随后作者又进行了两轮突变、组合和筛选,最终获得最佳突变体为MorB-Y72T-C191G-T240E-R110L-V73D-S34Q(命名为MorB-B3),转化率为95%,对映体比为95:5。
随后,作者研究了MorB-B3的底物谱。对于α-溴代芳香酮,该酶可以催化对位和间位有取代基的底物,供电子取代基的转化率比吸电子取代基的高;邻位取代方面,如果取代基较小,MorB-B3仍然可以催化;对于更大的芳香基团,如萘、苯并呋喃,MorB-B3也可催化反应发生。
对于烯烃方面,大的吸电子取代基会对反应产生负面影响,而三取代烯烃、非苯乙烯均可发生反应。
接着,作者做了一系列实验以探究反应机理。依据该类酶的特征,自由基的引发阶段应当是由酶模板的电荷转移复合物(enzyme-templated charge transfer complex)作用。但是作者发现,紫外-可见光并不能检测到该复合物,这是由于即使在非光照条件下,底物的结合也可使黄素自由基氧化。那么自由基是如何淬灭的呢?作者提出了两种猜想:一是过渡态1被氧化为阳离子的过渡态2,这个过程不成环;二是过渡态1发生环化形成过渡态3,形成氧自由基,随后水解。为了探究究竟是哪个机理,作者设计了苯环上又羟甲基取代的底物36,如果反应遵从第一种机理,那么会形成五元氧环的副产物。然而实际检测中,该副产物的含量极低,故该反应并非按第一种机理发生。作者又设计了邻位取代为羧酸或甲酯基团的底物38和39,若反应遵从第二种机理,那么羧酸或甲酯的羰基会与氧自由基反应形成内酯。实际检测中确实检测到了内酯的生成,故应当为第二种机理。
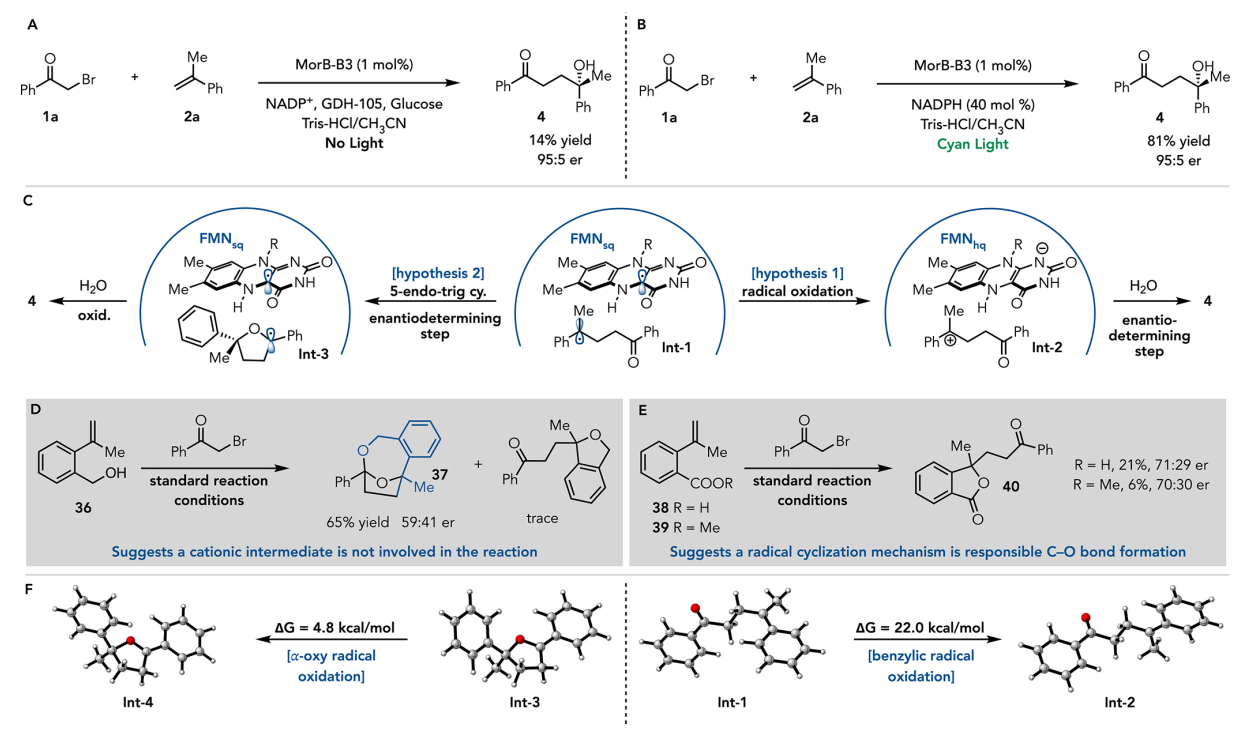
作者又进行了过渡态计算,计算结果表明过渡态1氧化形成过渡态2,比过渡态3形成过渡态4需要克服的能量高很多。该结果也支持第二种机理。
总结与展望
本文开发了一种通过光酶催化烯烃羰基羟基化反应不对称合成叔醇的方法。这篇文章的idea需要很强的化学功底和想象力,作者从反应机理出发,把两个看上去相去甚远的反应(加氢烷基化和羰基羟基化)联系到了一起,即“透过现象看本质”,在EREDs的作用中,自由基引发和C-C键的形成均是相同的,区别就在于最终的自由基淬灭。作者大胆的猜想了EREDs对于这种反应的潜力,做了一系列实验进行验证,并且巧妙地设计了底物讨论了反应机理。这项工作对开发酶的潜力,解锁“旧”酶的新反应提供了很好的启示。
参考文献
1. Ouyang, Y.; Turek-Herman, J.; Qiao, T. Z.; Hyster, T. K., Asymmetric Carbohydroxylation of Alkenes Using Photoenzymatic Catalysis. J Am Chem Soc 2023, 145 (31), 17018-17022.
-------
编译:江淮之间
编辑:LJJ
欢迎合成生物学领域科研从业者扫码加群成为专委会志愿者,解锁超多福利!加好友请备注“姓名+学历+专业”(不加备注不予通过)↓↓↓








